Quali sono gli elementi nel corpo umano?
 Share
Share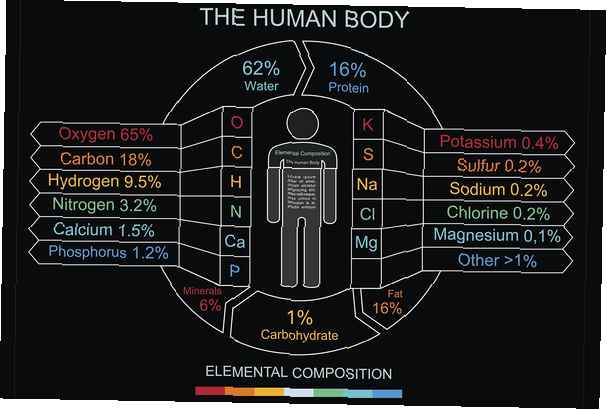
Esistono diversi modi per considerare la composizione del corpo umano, inclusi gli elementi, il tipo di molecola o il tipo di cellule. Gran parte del corpo umano è costituito da acqua, H2O, con cellule costituite per il 65-90% di acqua in peso. Pertanto, non sorprende che la maggior parte della massa di un corpo umano sia ossigeno. Il carbonio, l'unità di base per le molecole organiche, arriva secondo. Il 99% della massa del corpo umano è costituito da soli sei elementi: ossigeno, carbonio, idrogeno, azoto, calcio e fosforo.
- Ossigeno (O) - 65% - Ossigeno insieme all'idrogeno forma acqua, che è il solvente primario presente nel corpo e viene utilizzato per regolare la temperatura e la pressione osmotica. L'ossigeno si trova in molti composti organici chiave.
- Carbonio (C) - 18% - Il carbonio ha quattro siti di legame per altri atomi, il che lo rende l'atomo chiave per la chimica organica. Le catene di carbonio sono utilizzate per costruire carboidrati, grassi, acidi nucleici e proteine. La rottura dei legami con il carbonio è una fonte di energia.
- Idrogeno (H) - 10% - L'idrogeno si trova nell'acqua e in tutte le molecole organiche.
- Azoto (N) - 3% - L'azoto si trova nelle proteine e negli acidi nucleici che compongono il codice genetico.
- Calcio (Ca) - 1,5% - Il calcio è il minerale più abbondante nel corpo. È usato come materiale strutturale nelle ossa, ma è essenziale per la regolazione delle proteine e la contrazione muscolare.
- Fosforo (P) - 1,0% - Il fosforo si trova nella molecola ATP, che è il vettore di energia primaria nelle cellule. Si trova anche nelle ossa.
- Potassio (K) - 0,35% - Il potassio è un elettrolita importante. È usato per trasmettere impulsi nervosi e regolazione del battito cardiaco.
- Zolfo (S) - 0,25% - Due aminoacidi includono zolfo. I legami delle forme di zolfo aiutano a dare alle proteine la forma di cui hanno bisogno per svolgere le loro funzioni.
- Sodio (Na) - 0,15% - Il sodio è un elettrolita importante. Come il potassio, viene utilizzato per la segnalazione nervosa. Il sodio è uno degli elettroliti che aiuta a regolare la quantità di acqua nel corpo.
- Cloro (Cl) - 0,15% - Il cloro è un importante ione (anione) a carica negativa utilizzato per mantenere l'equilibrio dei fluidi.
- Magnesio (Mg) - 0,05% - Il magnesio è coinvolto in oltre 300 reazioni metaboliche. È usato per costruire la struttura di muscoli e ossa ed è un cofattore importante nelle reazioni enzimatiche.
- Ferro (Fe) - 0,006% - Il ferro si trova nell'emoglobina, la molecola responsabile del trasporto di ossigeno nei globuli rossi.
- Rame (Cu), Zinco (Zn), Selenio (Se), Molibdeno (Mo), Fluoro (F), Iodio (I), Manganese (Mn), Cobalto (Co) - totale inferiore allo 0,70%
- Litio (Li), Stronzio (Sr), Alluminio (Al), Silicio (Si), Piombo (Pb), Vanadio (V), Arsenico (As), Bromo (Br) - presenti in tracce
Molti altri elementi possono essere trovati in quantità estremamente ridotte. Ad esempio, il corpo umano contiene spesso tracce di torio, uranio, samario, tungsteno, berillio e radio. Gli elementi in tracce considerati essenziali nell'uomo includono zinco, iodio, probabilmente silicio, probabilmente boro, selenio, probabilmente nichel, cromo, manganese, litio, forse arsenico, molibdeno, cobalto e forse vanadio.
Non tutti gli elementi presenti nel corpo sono essenziali per la vita. Alcuni sono considerati contaminanti che sembrano non danneggiare, ma non svolgono alcuna funzione nota. Esempi includono cesio e titanio. Altri sono attivamente tossici, tra cui mercurio, cadmio e elementi radioattivi. L'arsenico è considerato tossico per l'uomo, ma svolge una funzione in altri mammiferi (capre, ratti, criceti) in tracce. L'alluminio è interessante perché è il terzo elemento più comune nella crosta terrestre, ma non ha alcuna funzione nota nelle cellule viventi. Mentre il fluoro viene utilizzato dalle piante per produrre tossine protettive, non svolge alcun ruolo biologico essenziale negli esseri umani.
Potresti anche voler visualizzare la composizione elementale di un corpo umano medio in massa.
fonti
- Chang, Raymond (2007). Chimica, 9a edizione. McGraw-Hill. ISBN 0-07-110595-6.
- Emsley, John (2011). Nature's Building Blocks: A-Z Guide to the Elements. OUP Oxford. p. 83. ISBN 978-0-19-960563-7.
- Frausto Da Silva, J. J. R; Williams, R. J. P (2001-08-16). La chimica biologica degli elementi: la chimica inorganica della vita. ISBN 9780198508489.
- H.A., V. W. Rodwell; P. A. Mayes, Revisione di chimica fisiologica, 16a edizione, Lange Medical Publications, Los Altos, California 1977.
- Zumdahl, Steven S. e Susan A. (2000). Chimica, 5a edizione. Houghton Mifflin Company. p. 894. ISBN 0-395-98581-1.
